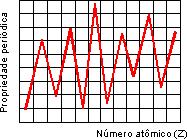
Propriedades periódicas são aquelas que crescem e decrescem em intensidade à medida que aumenta o número atômico.
|
|
|
|
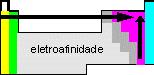
É a tendência que possui o átomo do elemento químico em atrair elétrons. |
Cresce de acordo com a eletronegatividade do elemento químico. |
|
|
|
|
Cresce de acordo com a eletronegatividade do elemento químico. |
É a energia liberada pelo átomo isolado do elemento químico no estado gasoso ao receber um elétron, dando um íon ânion gasoso. |
|
|
|
|
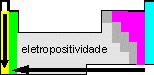
É a tendência que possui o átomo do elemento químico em ceder elétrons. |
Cresce de acordo com a eletropositividade do elemento químico. |
|
|
|
|
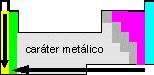
Cresce de acordo com a eletropositividade do elemento químico. |
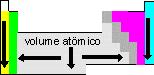
Depende do número de camadas eletrônicas e do número de prótons. |
|
|
|
|
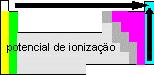
Éa energia necessária para remover um elétron do átomo do elemento químico no estado gasoso. |
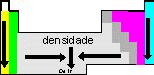
d = m / V |
|
|
|
|
V = m/d |
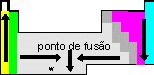
Passagem do estado físico sólido para o estado líquido do elemento químico. |